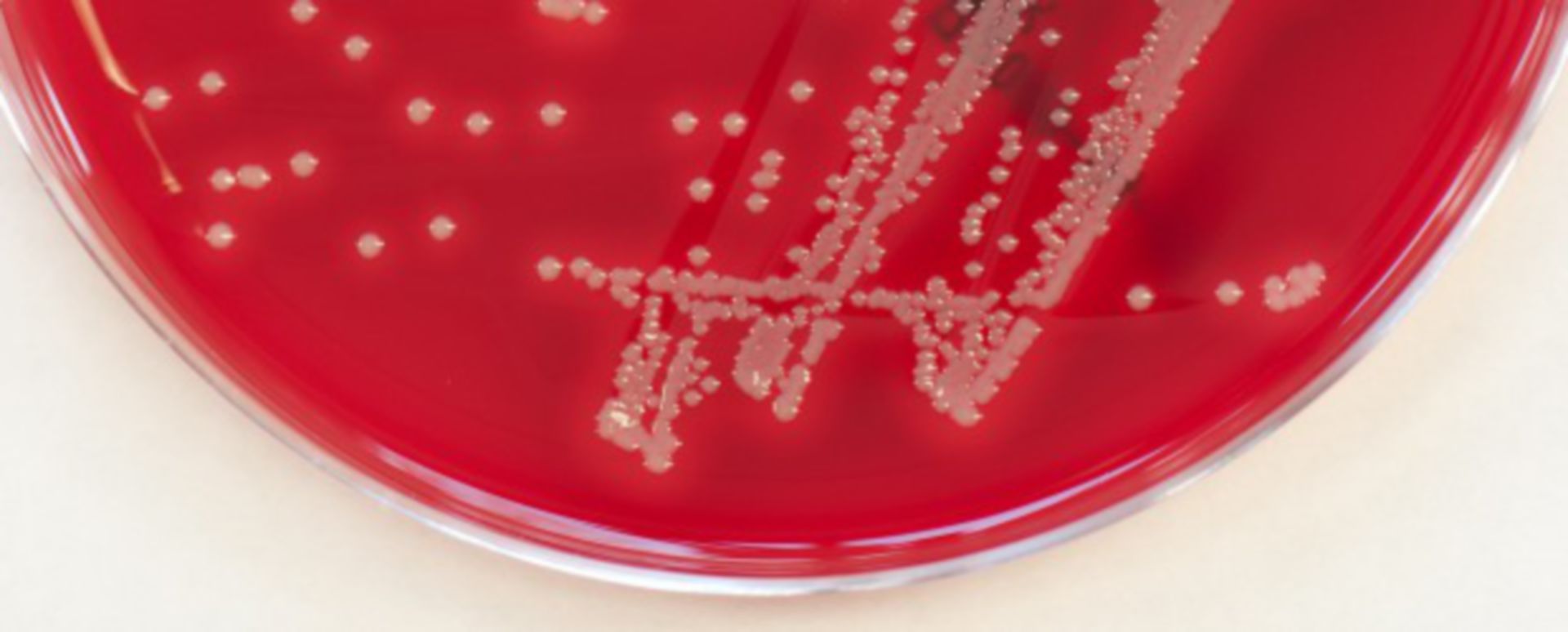
Mikroorganismen beeinflussen unser gesamtes Umfeld – in der Entstehung von Krankheiten oder auf unserer eigenen Haut. Bakterien und Pilze spielen in fast jeder Umgebung eine Rolle und haben mit der Zeit Anpassungsmechanismen entwickelt, die sie vor Umwelteinflüssen oder Antibiotika schützen.
Bei der Behandlung von chronischen Wunden ist diese Fähigkeit bedeutsam, da der Biofilm dadurch die Abheilung der Wunde verhindert.
Als Biofilm bezeichnet man eine Ansammlung von Mikroorganismen, die durch starke Vermehrung auf einer Oberfläche eine mikrobielle Gemeinschaft bilden. Durch Absonderung von speziellen Substanzen entsteht ein zusätzlicher Schutz für die Organismen. Die Bildung eines Biofilms läuft in folgenden Schritten ab:
- Anheften einzelner Organismen an die Oberfläche
- Vermehrung und stärkeres Anheften der Organismen sowie Veränderung des genetischen Musters
- Absonderung der Substanzen, die eine umhüllende Schicht bilden
Abhängig von den Organismen im Biofilm, geht die Bildung unterschiedlich schnell vonstatten. Aus den ersten angehefteten Mikroorganismen entwickelt sich innerhalb von zwei bis vier Stunden eine Kolonie, die in ungefähr sechs bis acht Stunden den Schutzfilm produziert. Nach zwei bis vier Tagen können dann neu entwickelte Resistenzen der mikrobiellen Gemeinschaft beobachtet werden. Durch die schnelle Entwicklung ist ein schnelles Handeln bei der Handhabung von Biofilmen, vor allem im Krankenhaus-Umfeld, besonders wichtig. [1]
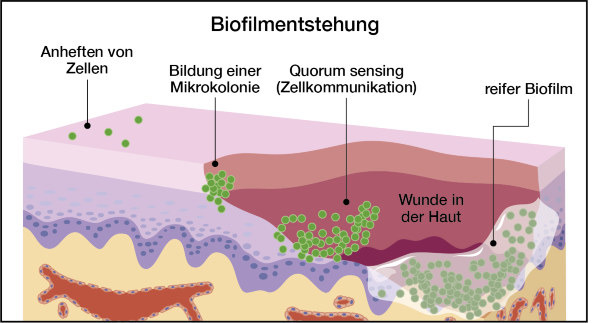
© Legger | Dreamstime.com
Die Bildung eines Biofilms birgt für die bewohnenden Organismen eine Reihe an Vorteilen. Zum einen wird die Immunabwehr des Patienten durch die aus Zuckermolekülen und Proteinen bestehende Schutzschicht abgeschwächt. Zum anderen ist der Biofilm aufgrund von polymeren Molekülen, die mehr oder weniger undurchlässig für antimikrobielle Substanzen sind, geschützt. Durch horizontalen Gentransfer, also die Übertragung von Genen zwischen den Zellen wird die Übertragung von Resistenzen zwischen den einzelnen Mikroorganismen gefördert, was den Biofilm noch widerstandsfähiger macht. [2]
Der Biofilm als medizinisches Risiko
Biofilme entstehen durch eine Vielzahl von Bakterien, die in der natürlichen Flora des Menschen vorkommen oder in medizinischen Einrichtungen, wie Krankenhäusern, infektionsbedingt eine große Rolle spielen. Beispielsweise findet man häufig Staphylokokken oder Pseudomonaden in Biofilmen, ebenso sind Enterobacteriaceae, z.B. im Darm zu findende E. coli, häufig Biofilmbildner. [1]
Im medizinischen Umfeld ist die Bildung eines Biofilms gerade an offenen Körperstellen, wie Wunden, ein Problem. Besonders bei immunsupprimierten Patienten kommt es häufig zur Bildung eines Biofilms, da das Immunsystem von Beginn der Besiedelung an zu schwach ist, die Mikroorganismen zu bekämpfen. Die Bildung eines Biofilms ist auch abhängig von der Art der Wunde. Laut Studien sind mehr als 60% aller chronischen Wunden durch Biofilme besiedelt. [1,3] Bei akuten Wunden handelt es sich um lediglich 6%. [1,3]
Möglicherweise kann die Chronizität der Wunde durch die dauerhafte Besiedelung mit biofilmbildenden Bakterien erklärt werden, da ein Abheilen der Wunde verhindert wird. Die Bakterien oder Pilze im Biofilm sorgen für eine konstante chronisch-entzündliche Reaktion, was zu vermehrter Bildung von Makrophagen und Granulozyten führt. Diese sondern unter anderem Proteasen ab, die schädigend gegenüber gesundem Gewebe, sowie Proteinen oder Immunzellen des Patienten sind. [3]
Behandlung infizierter Wunden
Vor der Behandlung eines Biofilms im medizinischen Umfeld muss sichergestellt werden, dass es sich um einen solchen handelt. Eine Wunde mit Wundbelag ähnelt dem Biofilm häufig, benötigt jedoch meist keine antibiotische Behandlung. Die optische Untersuchung zeigt bei Wundbelag meist eine trübe, viskose, gelbliche Flüssigkeit, wohingegen der Biofilm gelartig und glänzend erscheint. Die mikroskopische Untersuchung gibt weiteren Aufschluss darüber, welche Erreger an der Biofilm-Bildung beteiligt sind. [1]
Nach der Diagnose ist eine möglichst schnelle und vollständige Entfernung des Biofilms unerlässlich, um beim Patienten schneller ein Wohlbefinden zu erreichen. Die vollständige Entfernung des Biofilms ist dabei ein herausforderndes Unterfangen. Selbst ein gründliches chirurgisches Debridement ist keine Garantie für eine dauerhafte Biofilm-Entfernung, da nach einer mechanischen Zerstörung in nur 24 Stunden ein Wiederaufbau des Biofilms stattfinden kann. Das mechanische Debridement mit einem Monofilamentfaser-Pad stellt eine schnelle, sichere und einfache Alternative dar, die für den Patienten schmerzarm ist. Das vor der Behandlung angefeuchtete Pad nimmt Biofilm, Verunreinigungen, Nekrosen, Fibrin, Hyperkeratosen und andere Wundbeläge sowie abgestorbene Zellen aus dem Wundgrund in das Material auf und hält sie darin fest. Bereits neu eingewachsenes Granulationsgewebe und Epithelzellen werden geschont. So sorgt das Pad für ein sauberes Wundbett, welches eine wichtige Voraussetzung für die weitere Wundversorgung ist. Es ist bei vielen verschiedenen Wundtypen (z.B.: Diabetische Ulzera, arterielle und venöse Ulzera) einsetzbar. Dennoch kann sich auch nach Anwendung des mechanischen Debridement innerhalb von 24 Stunden erneut ein Biofilm aufbauen.
Die Wunde sollte regelmäßig durch eine Wundspüllösung mit Polihexanid (PHMB) gesäubert werden. Ebenso existieren Wundverbände, die mit PHMB angereichert sind und Wirksamkeit gegen ein besonders breites Erregerspektrum bieten. Bei einer Wundauflage mit PHMB wirkte das PHMB bereits in den ersten 6h gegen 99% der Keime. Wichtig dabei ist, dass das PHMB nicht nur im Verband, sondern auch in der Wunde wirkt. Auch silberhaltige Wundauflagen können bei der Heilung hilfreich sein, da die Silberionen den Biofilm durchdringen und die Mikroorganismen abtöten können.[3,4] Antimikrobielle Wundauflagen sollten jedoch bei infizierten Wunden alle 24 Stunden gewechselt werden. Zum Schutz vor Infektionen und Biofilm kann ein antimikrobielle Wundverband jedoch auch über mehrere Tage auf der Wunde verweilen.
Biofilme im medizinischen Umfeld bedeuten oft eine erschwerte Abheilung von Wunden. Daher ist eine sofortige Behandlung und eine optimale Vorbeugung von Infektionen essenziell.
Referenzen:
[1] Phillips P. L. et al. Biofilms made easy. Wounds International 2010;1(3)
[2] Costerton, J. W. et al Bacterial Biofilms: A Common Cause of Persistent Infections. Science 1999;284(5418): 1318-1322
[3] Streit, M. et al. Infections of chronic wounds. Zeitschrift für Wundheilung 2009;3: 160-176
[4] Hoppe H.-D. et al. Beläge auf chronischen Wunden – Fibrin, Nekrosen, Biofilm. Medizin & Praxis „Wunddébridement und Wundradpflege“ 2010: 28-31
Bildquelle:iStock/zmeel